Lernsituation 1 - Chemisch-physikalische Grundlagen: Unterschied zwischen den Versionen
Len (Diskussion | Beiträge) Keine Bearbeitungszusammenfassung |
Len (Diskussion | Beiträge) Keine Bearbeitungszusammenfassung |
||
| Zeile 102: | Zeile 102: | ||
Hier findest du einige '''Übungsaufgaben''', die zur '''Vertiefung''' und '''Kontrolle''' deiner neu erworbenen Kompetenzen im Lernfeld 8 dienen. Sie sind nach '''Kompetenzleveln aufgeteilt''', so kannst du den '''Schwierigkeitsgrad''' selbst steuern. | Hier findest du einige '''Übungsaufgaben''', die zur '''Vertiefung''' und '''Kontrolle''' deiner neu erworbenen Kompetenzen im Lernfeld 8 dienen. Sie sind nach '''Kompetenzleveln aufgeteilt''', so kannst du den '''Schwierigkeitsgrad''' selbst steuern. | ||
Aktuelle Version vom 23. Januar 2023, 20:29 Uhr
Wir Zahntechniker beherrschen mit dem Werkstoff Metall die komplette Palette der Fertigungsverfahren (Fertigungsverfahren in Wikipedia). Wir gießen Kronen (Urformen), biegen Klammern (Umformen), bearbeiten Oberflächen mit Fräsen (Trennen), löten und lasern (Fügen), vergolden Modellgussplatten (Beschichten) und härten Brückengerüste durch Wärmebehandlung (Stoffeigenschaften ändern).
Mit Ausnahme des Trennens, das Thema im Lernfeld Oberflächenbearbeitung ist, werden alle anderen Fertigungsverfahren in diesem Lernfeld erarbeitet.
Zu Beginn sollten wir uns mit den grundlegenden chemischen und physikalischen Eigenschaften der Metalle beschäftigen. Du findest hinter den Links zur Online-Enzyklpädie Wikipedia jeweils weiterführende Informationen.
Eigenschaften
80% aller Elemente des Periodensystems sind Metalle. Es werden Metalle (Alkali-, Erdalkali- und Übergangsmetalle) sowie Halbmetalle unterschieden. (Wikipedia Metalle, Wikipedia Periodensystem).
Typische chemische Eigenschaften der Metalle:
- Metalle haben relativ wenig Elektronen auf der äußersten Elektronenhülle (E.-Schale).
- Sie bilden daher leicht Ionen (Wikipedia Ionen)
Typische pysikalische Eigenschaften der Metalle:
- Außer Quecksilber sind sie bei Raumtemperatur alle fest. (Wikipedia Aggregatzustand)
- Ihre Oberfläche hat metallischen Glanz.
- Sie sind undurchsichtig.
- Sie sind dehnbar bzw. plastisch verformbar. (Wikipedia Duktilität, Kaltverfestigung)
- Sie haben eine gute thermische und elektrische Leitfähigkeit. (Wikipedia Leiter).
Metalle, die in den Hauptgruppen des PSE eingeordnet sind, sind reaktionsfreudiger (Oxidation!) als solche aus den Nebengruppen. Nebengruppenmetalle gelten daher als edel, während die Hauptgruppenmetalle eher als unedel bezeichnet werden. Du hast im Lernfeld "Oberflächenbearbeitung" beim Versuch mit der Zitronenbatterien schon schon die Begriffe edel und unedel im Zusammenhang mit Metallen kennen gelernt. Im Zweifel kannst du den Versuch ja nochmal durchführen (Lernsituation 4 - Korrosion im Mund)!
Metallbindung
Metallatome in metallischen Festkörpern werden durch die Metallbindung zusammengehalten (Wikipedia Metallbindung). Prinzipiell liegen positive Atomrümpfe vor (Metallionen), die ihre Außenelektronen (Wikipedia Außenelektronen) an die Umgebung abgegeben haben. So existiert zwischen den positiven Metallionen ein negativ geladenes Elektronengas (Wikipedia Elektronengas), dass die Metallionen zusammen hält.
Metallgitter
Die Atomrümpfe der Metalleatome ordnen sich im festen Zustand in bestimmter geometrischer Form an. Sie ist je nach Metall unterschiedlich, sodass es verscheidene Möglichkeiten gibt, kugelförmige Atomrümpfe mehr oder weniger dicht zu packen. Es gibt z.B.
- kubisch-flächenzentrierte,
- kubisch-raumzentrierte oder
- hexagonale
Metallgitter Wikipedia Kristallgitter.
Die gute plastische Verformbarkeit ist auf die Gitterstruktur der Metalle zurückzuführen.
Gefüge
Im flüssigen Zustand sind Metalle und ihre Legierungen amorph. Beim Übergang in den festen Zustand bildet sich ein Metallgefüge.
Lernvideo (Unterrichtsmitschnitt) zu Gleitebenen und Versetzungen beim Umformen von Metallen.
Legierungen
Durch Mischen verschiedener Metalle verändern sich die Eigenschaften. So können Werkstoffe "kreiert" werden, die spezielle gewünschte Eigenschaften besitzen. Ein metallischer Werkstoff aus mindestens zwei Komponenten nennt man Legierung. Die genannten Beispiele für Metalle sollen nur verdeutlichen, dass es unterschiedliche Metalle sind. Sie sind unter Umständen nicht richtig.
- Teile Deine Klasse in Gruppen von 3-4 Lernenden auf. Jede Gruppe entscheidet sich für einen Kompetenzlevel. Es dürfen auch Level mehrfach gewählt werden.
- Schaue zunächst das Lernvideo auf deinem Level und mache dir Notizen.
- Bearbeite dann die jeweilige interaktive Übung in Moodle.
- Erstelle dann gemeinsam mit deiner Gruppe ein Plakat und bereite dich auf die Präsentation vor.
- Präsentiert Euch gegenseitig in einem sogenannten Galeriegang die Plakate und macht Euch Notizen.
Lernvideo
Level 1 - vollständige Löslichkeit im festen Zustand (z.B. Gold und Silber)
Level 2 - vollständiger Unlöslichkeit im festen Zustand (z.B. Zinn und Blei)
Level 3 und 4 - begrenzter Löslichkeit im festen Zustand (z.B. Kupfer und Aluminium)
Übungen
Hier findest du einige Übungsaufgaben, die zur Vertiefung und Kontrolle deiner neu erworbenen Kompetenzen im Lernfeld 8 dienen. Sie sind nach Kompetenzleveln aufgeteilt, so kannst du den Schwierigkeitsgrad selbst steuern.
Level 1
Gold und Silber bilden ein Legierungssystem mit vollständiger Löslichkeit im festen Zustand. Gold hat seinen Schmelzpunkt bei 1064,18 °C, Silber bei 961,78 °C. Beide bilden ein kubisch-flächenzentriertes Raumgitter.
- Was ist ein Ion?
- Skizziere die Metallbindung mit Metallionen und Elektronengas. Kennzeichne die jeweilige Ladung.
- Was bedeutet das Wort "Duktilität"?
- Skizziere das Metallgitter, in dem beide Metalle erstarren.
- Was passiert in einem Metallgitter bei plastischer Verformung?
- Skizziere eine Abkühlungskurve von reinem Gold.
- Beschrifte sie mit den Begriffen "fest", "flüssig" und "Schmelzpunkt".
- Skizziere das Zustandsdiagramm der Legierungen aus Gold und Silber.
- Beschrifte es mit den Begriffen "Soliduslinie" und "Liquiduslinie".
Hilfen zur Kontrolle deiner Antworten:
Level 2
Zinn und Blei bilden ein Legierungssystem mit vollständiger Unlöslichkeit im festen Zustand. Blei hat seinen Schmelzpunkt bei 327,43 °C, Zinn bei 231,93 °C. Blei bildet eine kubisch-flächenzentrierte Kristallstruktur, Zinn eine kubische. Bei 63 % Zinn und 37 % Blei bildet die Legierung der beiden Metalle mit einer Schmelztemperatur von 183 °C ein Eutektikum.
- Skizziere die Metallbindung am Beispiel Zinn. Kennzeichne die Bestandteile und jeweiligen Ladungen.
- Erkläre den Begriff "Duktilität"?
- Skizziere jeweils die Kristallstruktur, in der beide Metalle erstarren und vergleiche sie mit einer kubisch-raumzentrieren Struktur.
- Skizziere die Vorgänge in einem Metallgitter bei plastischer Verformung.
- Skizziere eine Abkühlungskurve von reinem Zinn und eine Abkühlungskurve einer etwa 50/50-Blei-Zinn-Legierung.
- Beschrifte die Abkühlungskurven mit den Begriffen "fest", "flüssig", "Schmelzpunkt", "Liquiduspunkt", "Schmelzintervall" und "Soliduspunkt".
- Skizziere das Zustandsdiagramm der Legierungen aus Blei und Zinn.
- Beschrifte es mit den Begriffen "Soliduslinie", "Eutektikum" und "Liquiduslinie".
- Skizziere den kristallinen Aufbau eines Eutektikums und einer Legierung, die mehr Zinn enthält als das Eutektikum.
- Welche Bedeutung hat ein Eutektikum für deine zahntechnische Arbeit?
- Erläutere die Begriffe "Kristallgemisch" und "Mischkristall".
Level 3
Kupfer und Aluminium bilden ein Legierungssystem mit begrenzter Löslichkeit im festen Zustand. Kupfer hat seinen Schmelzpunkt bei 1084,62 °C, Aluminium bei 660,2 °C. Beide Metalle bilden eine kubisch-flächenzentrierte Kristallstruktur. Aluminium bildet mit Kupfer ein Eutektikum bei 547 °C und 5,7% Kupfer.
- Erläutere das Prinzip der Metallbindung mit Fachbegriffen
- Erläutere die Eigenschaft "duktil" und grenze Sie zur Eigenschaft "spröde" ab?
- Skizziere die dir bekannten Kristallstruktur und beschreibe diese kurz.
- Skizziere die Vorgänge in einem Metallgitter bei mehrmaliger plastischer Verformung in verschiedenen Richtungen.
- Skizziere eine Abkühlungskurve von reinem Aluminium und eine Abkühlungskurve einer etwa 20/80-Kupfer-Aluminium-Legierung und beschrifte sie mit allen Fachbegriffen.
- Skizziere das Zustandsdiagramm der Legierungen aus Aluminium und Kupfer und beschrifte es vollständig. Die Bereiche der Mischkristallbildung rechts und links und der Eutektikalen kannst du einfach grob schätzen.
- Skizziere den kristallinen Aufbau des Eutektikums und sechs weiterer Bereiche unterhalb der Soliduslinie.
- Welche Bedeutung hat ein Eutektikum für deine zahntechnische Arbeit?
- Erläutere die Begriffe "Kristallgemisch" und "Mischkristall".
Level 4
Kupfer und Aluminium bilden ein Legierungssystem mit begrenzter Löslichkeit im festen Zustand. Kupfer hat seinen Schmelzpunkt bei 1084,62 °C, Aluminium bei 660,2 °C. Beide Metalle bilden eine kubisch-flächenzentrierte Kristallstruktur. Aluminium bildet mit Kupfer ein Eutektikum bei 547 °C und 5,7% Kupfer.
- Erläutere das Prinzip der Metallbindung mit Fachbegriffen
- Erläutere die Eigenschaft "duktil" und grenze Sie zur Eigenschaft "spröde" ab?
- Skizziere die Kristallstruktur, in der beide Metalle erstarren und vergleiche sie mit einer hexagonalen Struktur.
- Skizziere die Vorgänge in einem Metallgitter bei mehrmaliger plastischer Verformung in verschiedenen Richtungen.
- Skizziere eine Abkühlungskurve von reinem Aluminium und eine Abkühlungskurve einer etwa 20/80-Kupfer-Aluminium-Legierung und beschrifte sie mit allen Fachbegriffen.
- Skizziere das Zustandsdiagramm der Legierungen aus Aluminium und Kupfer und beschrifte es vollständig. Die Bereiche der Mischkristallbildung rechts und links der Eutektikalen kannst du einfach grob schätzen.
- Skizziere den kristallinen Aufbau des Eutektikums und vier weiterer Bereiche unterhalb der Soliduslinie.
- Welche Bedeutung hat ein Eutektikum für deine zahntechnische Arbeit?
- Erläutere die Möglichkeit, eine solche Legierung durch nachträgliche Behandlung zu homogenisieren.
- Erläutere die Begriffe "Kristallgemisch" und "Mischkristall" und ordne sie den Bereichen des Zustandsdiagramms zu.
Weiterführende Links:
- Werkstoffkunde Metall auf de.wikibook.org
- Packungsdichte auf Wikipedia.de
Alte Inhalte:
(ALT) Lernvideo (Unterrichtsmitschnitt) zu Gitterstrukturen von Metallen.
Arbeitsauftrag:
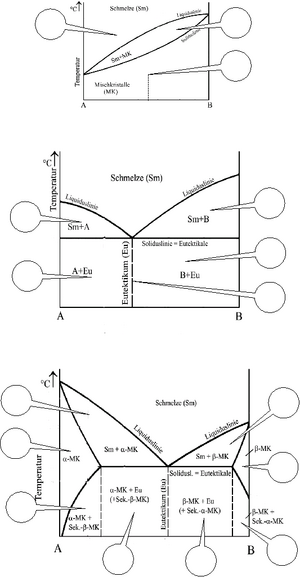
Drucke dir die drei Grafiken unten aus (bzw. benutze die ausgeteilten Arbeitsblätter) und fülle die Kreise jeweils mit dem Zustand der Legierung in der jeweiligen Phase aus. Du solltest aus deinen Skizzen genau erkennen können, welche Kristalle in der Legierung vorliegen und woraus sich die evtl. Restschmelze zusammensetzt. Als Vorlage dienen dir die Grafiken im Kapitel "Übersicht von Gefügeschliffbildern" unter Wikipedia Gefüge. Erklärungen zu den verschiedenen Legierungarten findest du unter Wikipedia Legierungen und in deinen Unterlagen!
Lernvideo (Unterrichtsmitschnitt) zu Legierungssystemen mit vollständiger Löslichkeit im festen Zustand (Level 1).
Lernvideo (Unterrichtsmitschnitt) zu Legierungssystemen mit vollständiger Unöslichkeit im festen Zustand (Level 2).
Lernvideo zu Legierungssystemen mit beschränkter Löslichkeit im festen Zustand (Level 3/4).