Info Metalleigenschaften normal
Legierung und Fertigungsverfahren
Legierungen sind Verbindungen von mindestens zwei Elementen, wobei mindestens eines davon ein Metall sein muss. Die anderen Elemente können entweder Metalle oder Nichtmetalle sein. Legierungen werden durch die Metallbindung zusammengehalten.
Aber was sind überhaupt Metalle? Und wie bringt man Legierungen und Metalle dazu, sich in die gewünschte Form zu bringen? Um dies zu klären, können wir uns erstmal überlegen, wo wir Metalle nutzen und wie wir diese nutzen.
Dabei ist es hilfreich, sich die verschiedenen Fertigungsverfahren anzuschauen. Diese können aufgrund ihres Zusammenhaltes der Atome unterschieden werden. So wird z.B. bei Urformen der Zusammenhalt geschaffen. Es gab vorher keinen Zusammenhalt (z.B. Flüssig, Gasförmig, Pulver) und nach der Anwendung des Fertigungsverfahrens gibt es ein Zusammenhalt. Der Zusammenhalt wurde somit geschaffen. Weitere Informationen finden Sie auf Wikipedia unter diesem Link: Fertigungsverfahren
Elektronengasmodell bei Metallen
Metalle können bezüglich ihrer chemischen und physikalischen Eigenschaften im flüssigen und festen Zustand definiert werden.
Diese Eigenschaften sind:
- Elektrische Leitfähigkeit
- Thermische Leitfähigkeit
- Metallischer Glanz
- Verformbarkeit
- Metallbindung
Diese Eigenschaften werden durch das Elektronengasmodell beschrieben.
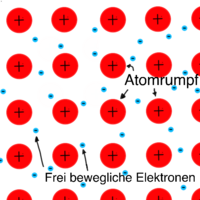
Das Elektronengasmodell beschreibt Metalle als eine Anordnung von positiv geladenen Atomkernen mit einem „Gas“ von frei beweglichen Valenzelektronen. Diese (Valenz-)Elektronen sind nicht an ein bestimmtes Atom gebunden und können sich stattdessen frei durch die gesamte Metallstruktur bewegen.
Das Elektronengasmodell bietet ein grundlegendes Verständnis der einzigartigen physikalischen und chemischen Eigenschaften von Metallen. Es betont die freie Bewegung von Valenzelektronen innerhalb der Metallstruktur und erklärt, warum Metalle gute elektrische und thermische Leiter sind, formbar sind und einen metallischen Glanz haben. Komplexere Modelle wie das Bandmodell berücksichtigen zusätzliche Details, dies ist für uns jedoch nicht notwendig.
Eigenschaften, die durch das Elektronengasmodell (vereinfacht) erklärt werden
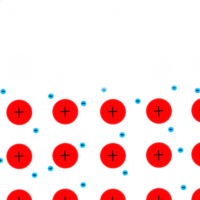
- Elektrische Leitfähigkeit: Die freien Elektronen in Metallen ermöglichen den Transport von elektrischem Strom. Wenn eine Spannung angelegt wird, fließen die Elektronen in eine Richtung und leiten den Strom.
- Thermische Leitfähigkeit: Wenn die Temperatur in einem Metall erhöht wird, beginnen die Atomkerne sich stärker zu bewegen. Dabei stoßen sie mit den frei beweglichen Elektronen, die im Elektronengas vorhanden sind, zusammen. Diese Zusammenstöße führen dazu, dass sich auch die Elektronen stärker bewegen. Die Energie dieser Bewegung wird durch das Elektronengas auf die benachbarten Atomkerne übertragen, und so breitet sich die erhöhte Bewegung allmählich im gesamten Metallgitter aus. Diese verstärkte Teilchenbewegung führt zu einer Erhöhung der Temperatur, die wir als Wärme wahrnehmen. (Mehr dazu später) Link: Animation der thermischen Leitfähigkeit auf LEIFI Physik
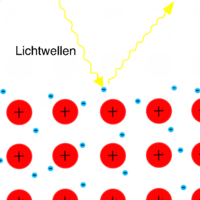
- Metallischer Glanz: Metalle reflektieren Licht, was ihnen ihren charakteristischen Glanz verleiht. Dies liegt an der Wechselwirkung des Lichts mit den freien Elektronen.
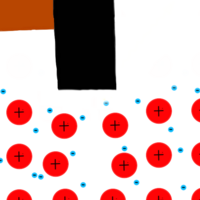
- Verformbarkeit: Wenn auf ein Metall Druck ausgeübt wird, rücken die positiv geladenen Atomkerne näher zusammen. Sie würden sich normalerweise gegenseitig abstoßen, da sie dieselbe positive Ladung haben. Doch das Elektronengas, das zwischen den Atomkernen vorhanden ist, hält sie weiterhin zusammen. Es wirkt wie eine verbindende Kraft, die verhindert, dass die Atomkerne sich trotz ihrer Nähe voneinander entfernen. (Mehr dazu später)
- Metallbindung: Die Anziehung zwischen den positiv geladenen Atomkernen und den frei beweglichen Elektronen erzeugt eine Bindung, die als metallische Bindung bekannt ist, die das Metall zusammenhält. (Mehr dazu später)
Übung
Lernender des ADBK-Düsseldorfs? Dann finden Sie die interaktive Übung in Moodle.
(Level 4 Extras) Technischer, wirtschaftlicher und ökologischer Nutzen von Metallen
Der Nutzen von Metallen kann in verschiedene Kategorien eingeteilt werden:
Technischer Nutzen
In Technik und Industrie müssen Materialien oft ganz bestimmte Eigenschaften haben. Dazu muss man manchmal verschiedene Eigenschaften kombinieren, um das Material genau passend zu machen (legieren). Diese Mischung aus verschiedenen Eigenschaften nennt man technische Eigenschaften. Außerdem muss das Material so bearbeitet werden können, dass es die richtige Form bekommt. Das kann unter anderen durch Schmelzen und Gießen oder durch Fräsen und Biegen passieren.
Wirtschaftlicher Nutzen
Technische Eigenschaften sind vielleicht nicht so wichtig, wenn das Material zu teuer ist oder nicht in ausreichenden Mengen erhältlich ist. Ein Metall wird nur dann verwendet, wenn es nützliche technische Eigenschaften hat und es gleichzeitig kosteneffizient ist, es herzustellen und zu verarbeiten. Ob ein Metall aus wirtschaftlicher Sicht interessant ist, sieht man oft daran, wie viel davon produziert wird.
Ökologischer Nutzen
Metalle sollten so verwendet werden, dass sie mit den Bedürfnissen der Menschen im Einklang stehen, nicht nur jetzt, sondern auch in der Zukunft. Das bedeutet, dass sie leicht recycelbar sein sollten. Recycling ist bei Metallen üblich, weil es viel billiger und einfacher ist als die Gewinnung aus Erz. Das Einschmelzen eines Metalls kostet nur einen Bruchteil der Energie und des Geldes, die für die ursprüngliche Gewinnung benötigt werden. In einem Schmelzofen können verschiedene Metalle getrennt und in neue Formen gegossen werden. Einige spezielle Legierungselemente, die sich ähnlich verhalten, können jedoch schwer oder nur mit viel Aufwand getrennt werden.