Lernsituation 3 - Das Elektrolytische Glänzen
Das elektrolytischen Glänzen (Elektrolyse in Wikipedia) ist ein Vorgang zur Oberflächenbearbeitung, der in der Modellgusstechnik für Partielle Prothesen verwendet wird. (Werbung für ein Glänzgerät der Firma BEGO)
Das gegossene, ausgebettete und abgestrahlte Objekt (meist eine Modellgussprothese) wird in das elektrolytischen Glänzbad gehängt. Das Gerät wird für eine bestimmte Zeit eingeschaltet. Nun fließt Strom durch den Elektrolyten, der die Spitzen des Rauhigkeitsprofils der Oberfläche des Objektes ganz langsam abträgt. Anschließend ist es glatter (hat also eine geringere Rauhigkeit) und glänzt! Das ist bei so einem komplexen Objekt viel einfacher und gleichmäßiger, als das Ausarbeiten mit Fräsen oder Schleifwerkzeugen.
Elektrolytisches Glänzen bei der Schmuckherstellung:
Bevor du verstehen kannst, was da im Glänzbad läuft, musst du dir ein paar Kompetenzen zum Thema "Chemie", speziell der "Protolyse", aneignen. Diese Protolyse macht der Hersteller des Elektrolyten, bevor ihr den Kanister mit dem Zeugs kauft. Der Elektrolyt verbraucht sich nämlich und muss regelmäßig ausgetauscht wereden, dazu aber später mehr.
Arbeitsauftrag 1:
Folge dem Link Elektrolyt und erstelle dir aus den dortigen Informationen eine Ablaufschema zur Entstehung von Elektrolyten. Bitte evtl. deinen Lehrer um ein vorgefertigtes Arbeitsblatt zum Ausfüllen
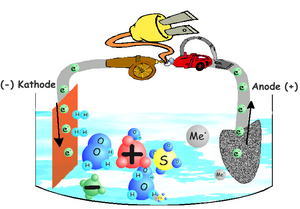
Prinzipiell passiert in einem Glänzbad folgendes:
Durch eine von außen angelegte elektrische Spannung (Gleichstrom) wird an einer mit dem Pluspol verbundenen Elektrode (unser Werkstück, die Modellgussprothese) ein Elektronenmangel ("Elektronensog") und einer mit dem Minuspol verbundenen Elektrode (Kupferplatten im Glänzbad) ein Elektronenüberschuss ("Elektronendruck") erzeugt. Die elektrochemische Oxidation erfolgt an der Anode und besteht in einem Elektronenentzug durch die Stromquelle: Die Anode ist bei der Elektrolyse die positiv geladene Elektrode (Pluspol), die Kathode die negativ geladene Elektrode (Minuspol).
Damit der Vorgang dauerhaft abläuft, muss ständig Energie zugeführt werden. Dies geschieht in Form von elektrischem Gleichstrom, der der Anode ständig Elektronen entzieht (absaugt) und sie zur Kathode "pumpt".
Damit der Stromkreis geschlossen bleibt, muss im Elektrolyten ebenfalls Strom fließen. Hier wird der Ladungstransport durch Ionen erledigt: Die negativ geladenen Anionen sind in unserem Beispiel der Säurerest im Elektrolyten, sie wandern bevorzugt zur positiv geladenen Anode. Die positiv geladenen Kationen, hier Oxonium-Ionen, wandern zur negativ geladenen Kathode.
An der Kathode erhalten die Hydroniumionen ihr fehlendes Elektron zurück und steigen als Wasserstoffgas auf. Der Rest bleibt als Wasser zurück. An der Anode verbindet sich ein Säurerest mit einem Metallion aus der Oberfläche des dort befestigten Werkstücks. Sie bilden zusammen ein Salz, dass sich als Schlamm am Boden des Beckens sammelt. Durch das Entfernen der Metallionen aus dem Werkstück, bevorzugt von erhabenen Stellen der Oberfläche, wird dieses glatter und glänzt!
Die Ionen des Elektrolyten werden also verbraucht. Das erklärt die nachlassende Wirkung des Glänzbades und die Notwendigkeit des Austauchens des Glänzbades von Zeit zu Zeit.
Eine Animation des Ablaufs
verdeutlicht die Vorgänge beim elektrolytischen Glänzen!
Und ein Lernvideo dazu:
Arbeitsauftrag 2:
Erkläre mit Hilfe der obigen Texte, Bilder und der Animation schriftlich die Vorgänge beim Glänzen von Modellgussprothesen. Fertige dabei eine oder mehrere Skizzen des Vorgangs an. Natürlich kannst du auch gern eine Präsentation oder eine andere Form der Darstellung wählen. Kreativität ist nicht verboten ;-)!
Arbeitsauftrag 3:
Das Glänzbad in deinem Labor funktioniert nicht mehr richtig! Du versuchst, bei voller Stromstärke und maximaler Zeiteinstellung, eine Modellgussprothese zu glänzen, aber es passiert fast nichts auf der Oberfläche! Die Elektrolyt-Brühe sieht ziemlich dunkel aus ...
Arbeitsauftrag 4:
Ändere den Aufbau des Glänzbades anschließend so, dass nicht Material abgetragen sondern aufgetragen wird! (Geschieht z.B. beim elektrochemischen Vergolden von Werkstücken oder in der Galvanotechnik).
Alternatives Lernangebot:
Montag morgen, Ihr Chef hat verschlafen, erwartet aber einen Vertreter aus dem Dentaldepot, der ihm ein neues Glänzgerät vorführen soll. An der Türe klingelt es und Herr Müller, angereist aus Bremen steht vor der Tür. Unter dem Arm hat er das neue Glänzgerät Eltropol 300.
Alle anderen Mitarbeiter sind auf einmal schrecklich beschäftigt, und Ihr Ausbilder schlägt vor, dass Sie sich das Gerät vorführen lassen, da Sie sich ja in der Berufsschule mit dem Thema „Oberflächenbearbeitung“ beschäftigen. Sie sollen sich Notizen machen, um dem Chef später die Funktion des Gerätes erklären zu können. Herr Müller baut das Glänzgerät vor Ihnen auf und klemmt den sandgestrahlten Modellguss an, der tatsächlich hochglänzend aus dem Gerät wieder zum Vorschein kommt.
Mit der Theorie, die dahinter steckt, muss er leider passen…
Er ist noch nicht sehr lange im Betrieb und heute ausnahmsweise für seinen Kollegen eingesprungen, der krank geworden ist.
(Das im Unterricht verwendete Glänzbad entspricht in seiner Funktion dem Eltropol 300 – es handelt sich allerdings um ein stark vereinfachtes Modell zur Veranschaulichung der theoretischen Zusammenhänge.)
Arbeitsauftrag
Teil 1:
- Protokollieren Sie in Tandemgruppen (je 2 SchülerInnen) den Versuchsaufbau des Glänzbad-Modells auf der Rückseite des ausgeteilten Arbeitsblattes.
- Beschreiben Sie in Stichpunkten, was im Glänzbad geschieht.
- Fertigen Sie dazu eine Skizze an.
Teil 2: (erst nach der Besprechung des ersten Teils)
- Erklären Sie (in Stichpunkten) den Ablauf des elektrolytischen Glänzens.
- Ergänzen Sie dazu Ihre Skizze um die relevanten chemischen Prozesse.